度普利尤单抗五年留存率达74.1%,多数皮炎患者症状显著改善,安全性良好
伊顿健康导读:
特应性皮炎是一种常见的皮肤病,其病因复杂,涉及遗传、环境和免疫系统的多种因素。如果你正经历着皮肤干燥、瘙痒以及红斑等不适这些症状,那么你可能需要关注一下是否是特应性皮炎在作祟。
这些症状在严重的情况下,甚至有可能导致皮肤出现破损和感染。而且治疗起来相当困难,患者往往需要长期进行系统性的治疗。
近日,一项发表在《Journal of Dermatological Treatment》上的真实世界研究,公布了度普利尤单抗(Dupilumab)治疗重度特应性皮炎(AD)长达五年的疗效、安全性和药物留存率数据。该研究为评估其长期表现提供了重要证据。
一、度普利尤单抗治皮炎的实验过程
研究从2018年6月开始,至2023年11月结束。结果表明,患者症状和生活质量持续改善,使用EASI、P-NRS和DLQI等指标评估治疗效果。
研究涉及709名重度异位性湿疹患者,评估度普利尤单抗的持续使用情况及影响因素。
53.2%的患者为男性,中位年龄33.0岁(13-90岁)。治疗随访期为0-65个月。所有患者接受标准剂量度普利尤单抗治疗,基线剂量600 mg,后续每两周300 mg,部分患者每4周或每3周接受300 mg。
二、度普利尤单抗用于特应性皮炎完全清除
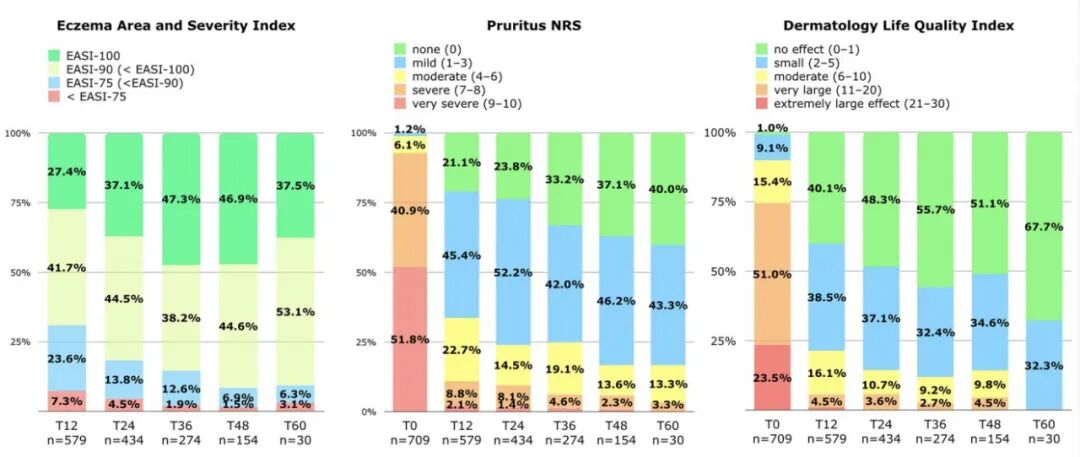
研究数据显示,中位EASI评分随治疗时间持续降低,证明治疗效果长期保持。
治疗60个月后,37.5%的患者皮肤损伤完全清除,90.6%的患者改善≥90%,96.9%的患者改善≥75%。
同时,83.3%的患者无瘙痒或仅轻微瘙痒,所有患者的生活品质受影响极小。P-NRS和DLQI评分显示症状和生活品质长期显著提升。
三、研究表明:度普利尤单抗药物持续率高
度普利尤单抗持续留存率高:超过八成患者长期坚持治疗药物持续留存率是衡量药物长期效果和耐受性的关键指标。
度普利尤单抗治疗12、24、48、60及65个月时,总体药物持续留存率分别为96.6%、93.4%、89.9%、84.2%和74.1%。
若仅考虑因治疗效果不足(原发性或继发性无效)而停药的情况,相应时间点的度普利尤单抗持续留存率更高,分别为98.8%、97.2%、95.8%、92.8%和86.4%。
若仅考虑因不良事件(AE)停药的情况,相应时间点的度普利尤单抗持续留存率分别为97.8%、96.4%、94.0%、91.7%和83.2%。
四、度普利尤单抗用药期间副作用微小
关注特定不良事件:部分表型与银屑病发生相关研究中,9名患者因出现银屑病而停药。研究显示:度普利尤单抗的副作用微小。
五、总结
统计分析显示,无异位性皮炎家族史的患者,因发生银屑病而停药的风险显著增加。除表型外,基线特征大多不影响药物留存率,但钱币状湿疹样是银屑病发生的一个重要预测因素。
度普利尤单抗治疗重症异位性湿疹具有长期的效果和安全性,五年药物持续留存率较高。研究结果为临床医生和患者对该药进行长期管理提供了坚实的数据支持。
临床招募分享:
目前有类似靶点的临床项目在开展,符合条件、用药、体检由申办方承担,不收取费用,同时会有交通补贴和营养补贴。
有需要的患者可以下方扫描客服二维码报名了解详情。

参考文献:
Barei F, Calzari P, Valtellini L, Chiei Gallo A, Perego G, Tavecchio S, Zussino M, Marzano AV, Ferrucci S. Five-year real-world drug survival of dupilumab in severe atopic dermatitis and associate predictors. J Dermatolog Treat. 2024 Dec;35(1):2404718. doi: 10.1080/09546634.2024.2404718. Epub 2024 Oct 13. PMID: 39396818.
本文仅做参考,不构成对任何药物或诊疗方案的推荐、推广或宣传,也不可替代专业医疗建议。如有问题,请咨询医疗卫生专业人士。材料图片等源自网络,侵删。